Enzymy
definicja
Enzymy to substancje chemiczne, które można znaleźć w całym organizmie. Wprawiają w ruch reakcje chemiczne w organizmie.
historia
Słowo enzym był z Wilhelm Friedrich Kühne 1878 i pochodzi od greckiego słowa enzymon, które oznacza drożdże lub zakwas. To następnie trafiło do międzynarodowej nauki. Plik międzynarodowy związek czystej chemii stosowanej (IUPAC) i międzynarodowy związek biochemii (IUBMB) opracowali nazewnictwo enzymów, które określa przedstawicieli tej dużej grupy substancji jako grupę wspólną. Nazewnictwo, które klasyfikuje enzymy zgodnie z ich zadaniami, jest ważne dla określenia zadań poszczególnych enzymów.
Ilustracja enzymów
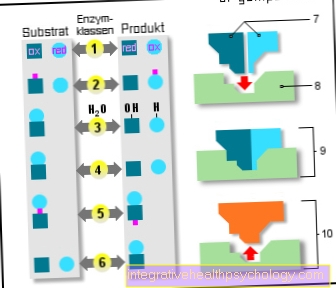
Enzymy
6 klas enzymów:
- Oksydoreduktazy
(Utlenianie / redukcja) - Transferazy
(Przenoszenie) - Hydrolazy
(Wykorzystanie wody) - Lyases
(Łupliwość) - Izomerazy
(ten sam wzór cząsteczkowy) - Ligazy
(Reakcje addycji) - Podłoża
- Centrum aktywne
- Enzym / substrat
złożony - Enzym / produkt
złożony
Przegląd wszystkichZdjęcia Dr-Gumperta można znaleźć pod adresem: ilustracje medyczne
Nazewnictwo
Plik Nazewnictwo enzym jest włączony trzy podstawowe zasady na podstawie.Nazwy enzymów kończące się na -azie opisują kilka enzymów w systemie. Sama nazwa enzymu opisuje reakcję, którą enzym wprawia w ruch (katalizowane). Nazwa enzymu jest również klasyfikacją enzymu. Ponadto system kodowania System numerów WE, w którym enzymy są wytwarzane pod kodem numerycznym cztery cyfry może być znaleziony. Pierwsza liczba wskazuje klasę enzymu. Listy wszystkich wykrytych enzymów zapewniają szybsze znalezienie określonego kodu enzymu. Chociaż kody są oparte na właściwościach reakcji katalizowanej przez enzym, w praktyce kody numeryczne okazują się nieporęczne. Częściej używane są nazwy systematyczne oparte na powyższych zasadach. Problemy z nazewnictwem pojawiają się na przykład w przypadku enzymów, które katalizują kilka reakcji. Dlatego czasami jest dla nich kilka nazw. Niektóre enzymy mają trywialne nazwy, które nie wskazują, że wspomniana substancja jest enzymem. Ponieważ nazwy były tradycyjnie szeroko używane, niektóre z nich zostały zachowane.
Klasyfikacja według funkcji enzymu
Według IUPAC i IUBMB, enzymy są podzielone na sześć klas enzymów w zależności od reakcji, którą inicjują:
- Oksydoreduktazy
Oksydoreduktazy wprawiają w ruch reakcje redoks. W tej reakcji chemicznej elektrony przechodzą od jednego partnera reakcji do drugiego. Następuje uwolnienie elektronów (utlenianie) z jednej substancji i wychwyt elektronów (redukcja) przez inną substancję.
Wzór katalizowanej reakcji to A ?? + B? A? + B?
Substancja A uwalnia elektron (?) I jest utleniana, podczas gdy substancja B absorbuje ten elektron i ulega redukcji. Dlatego reakcje redoks nazywane są również reakcjami utleniania-redukcji.
Wiele reakcji metabolicznych to reakcje redoks. Oksygenazy przenoszą jeden lub więcej atomów tlenu na swoje podłoże. - Transferazy
Transferazy przenoszą grupę funkcyjną z jednego podłoża na drugie. Grupy funkcyjne to grupy atomowe w związkach organicznych, które w dużym stopniu decydują o właściwościach substancji i zachowaniu się reakcji. Związki chemiczne, które mają takie same grupy funkcyjne, są pogrupowane w klasy substancji ze względu na ich podobne właściwości. Grupy funkcjonalne zostaną podzielone w zależności od tego, czy są heteroatomami, czy nie. Heteroatomy to wszystkie atomy w związkach organicznych, które nie są ani węglem, ani wodorem.
Np .: -OH -> grupa hydroksylowa (alkohole) - Hydrolazy
Hydrolazy rozszczepiają wiązania w odwracalnych reakcjach z użyciem wody. Estry, estry, peptydy, glikozydy, bezwodniki kwasowe lub wiązania C-C. Reakcja równowagi to: A-B + H2O? A-H + B-OH.
Enzym należący do grupy hydrolaz to m.in. Alfa galaktozydaza. - Lyases
Lazy, zwane również syntazami, katalizują rozszczepianie złożonych produktów z prostych substratów bez odszczepiania ATP. Schemat reakcji to A-B → A + B.
ATP to trifosforan adenozyny i nukleotyd, składający się z trifosforanu nukleozydu adenozyny (i jako taki bogaty w energię element budulcowy RNA kwasu nukleinowego). Jednak ATP jest przede wszystkim uniwersalną formą natychmiast dostępnej energii w każdym ogniwie i jednocześnie ważnym regulatorem procesów zaopatrzenia w energię. W razie potrzeby ATP jest ponownie syntetyzowany z innych magazynów energii (fosforan kreatyny, glikogen, kwasy tłuszczowe). Cząsteczka ATP składa się z reszty adeniny, rybozy cukrowej i trzech fosforanów (? To?) W wiązaniach estrowych (?) Lub bezwodnikowych (? A?). - Izomerazy
Izomerazy przyspieszają przemianę chemiczną izomerów. Izomeria to występowanie dwóch lub więcej związków chemicznych o dokładnie tych samych atomach (ten sam wzór empiryczny) i masach cząsteczkowych, które jednak różnią się połączeniem lub przestrzennym układem atomów. Odpowiednie związki nazywane są izomerami.
Izomery te różnią się pod względem chemicznym i / lub fizycznym, a często także właściwościami biochemicznymi. Izomeria występuje głównie w przypadku związków organicznych, ale także (nieorganicznych) związków koordynacyjnych. Izomeria jest podzielona na różne obszary. - Ligazy
Ligazy katalizują tworzenie się substancji, które są chemicznie bardziej złożone niż stosowane substraty, ale w przeciwieństwie do liaz są skuteczne tylko enzymatycznie w rozszczepianiu ATP. Tworzenie tych substancji wymaga zatem energii, która jest uzyskiwana w wyniku rozszczepienia ATP.
Niektóre enzymy są w stanie katalizować kilka, czasem bardzo różnych reakcji. W takim przypadku przypisuje się je do kilku klas enzymów.
Mogą Cię również zainteresować te artykuły:
- Alfa-glukozydaza
- Lipaza
- Trypsyna
Klasyfikacja według struktury enzymu
Prawie wszystkie enzymy są białkami i można je sklasyfikować według długości łańcucha białkowego:
- Monomery
Enzymy składające się tylko z jednego łańcucha białkowego - Oligomery
Enzymy, które składają się z kilku łańcuchów białkowych (monomerów) - Łańcuchy wieloenzymatyczne
Kilka zagregowanych enzymów, które współpracują i regulują się nawzajem. Te łańcuchy enzymatyczne katalizują kolejne etapy metabolizmu komórki.
Ponadto istnieją pojedyncze łańcuchy białkowe, które zawierają kilka aktywności enzymatycznych; są to nazywane enzymami wielofunkcyjnymi.
Klasyfikacja według kofaktorów
Inną klasyfikacją jest klasyfikacja oparta na uwzględnieniu kofaktorów. Kofaktory, koenzymy i kosubstraty to nazwy różnych klasyfikacji substancji, które wpływają na reakcje biochemiczne poprzez ich interakcję z enzymami.
Uwzględniono cząsteczki organiczne i jony (głównie jony metali).
Czyste enzymy białkowe składają się wyłącznie z białek, a centrum aktywne jest utworzone tylko z reszt aminokwasowych i szkieletu peptydowego. Aminokwasy to klasa związków organicznych z co najmniej jedną grupą karboksylową (-COOH) i jedną grupą aminową (-NH2).
Holoenzymy składają się ze składnika białkowego, apoenzymu i kofaktora, cząsteczki o niskiej masie cząsteczkowej (nie białka). Oba razem są ważne dla funkcji enzymu.
Koenzymy
Cząsteczki organiczne jako kofaktory nazywane są koenzymami. Jeśli są kowalencyjnie związane z apoenzymem, nazywane są grupami prostetycznymi lub kosubstratami. Grupa prostetyczna to termin używany do opisania składników niebiałkowych silnie (zwykle kowalencyjnie) związanych z białkiem o działaniu katalitycznym.
Kosubstraty to nazwy różnych klasyfikacji substancji, które wpływają na reakcje biochemiczne poprzez ich interakcję z enzymami. Jako biokatalizatory, cząsteczki przyspieszają reakcje w organizmach, enzymy przyspieszają reakcje biochemiczne. Zmniejszają energię aktywacji, którą należy pokonać, aby substancja mogła zostać przekształcona.