Biologia
wprowadzenie
Układ odpornościowy jest niezbędny do przetrwania każdego człowieka. W toku ewolucji rozwinęło się to w tak zwany adaptacyjny układ odpornościowy u ludzi. Daje nam to możliwość bardziej zróżnicowanej i skuteczniejszej reakcji na bakterie i wirusy. Chroni nas system odpornościowy. Pomaga nam lepiej przetrwać walkę z zapaleniem. Istnieje wiele różnych typów modulatorów zapalenia. Na przykład tak zwany czynnik martwicy nowotworów-alfa, który jest w skrócie TNF-α. Wraz z innymi czynnikami zapewnia to eliminację komórek zapalnych i nowotworowych, zanim zaczną one wywoływać choroby.

Ale ci „ochroniarze” naszego ciała mogą również stać się „przestępcami”. Ponieważ czasami nasz układ odpornościowy zwraca się przeciwko nam. W takich przypadkach rozwijają się choroby autoimmunologiczne, które trudno jest leczyć lekami. W tym miejscu wkraczają leki biologiczne. Biologie są również nazywane biofarmaceutykami lub biofarmaceutykami. Są to leki wytwarzane w organizmach zmodyfikowanych genetycznie przy użyciu różnych środków biotechnologicznych. Przykładami takich leków są tak zwane „przeciwciała monoklonalne” lub tak zwane „białka fuzyjne”. Do tej grupy leków należą inhibitory TNF-α, w tym antagoniści receptora TNF-alfa.
Dobrze znanym środkiem biologicznym jest adalimumab, znany również pod nazwą handlową Humira.
Wskazania
Antagoniści receptora TNF-α są wykorzystywani w zapalnych, przewlekłych chorobach autoimmunologicznych. Oznacza to, że są wskazane w przypadku wszystkich chorób, w których układ odpornościowy organizmu walczy z organizmem zamiast o niego walczyć. W tym procesie TNF-α często odgrywa główną rolę. Zapewnia, że określone komórki zaczynają zachowywać się jak tak zwane komórki padlinożerne (makrofagi), niszcząc w ten sposób tkanki, kości, chrząstkę i, w zależności od choroby, inne komórki organizmu.
Specyficznymi wskazaniami są na przykład reumatoidalne zapalenie stawów, tak zwane młodzieńcze idiopatyczne zapalenie stawów, łuszczycowe zapalenie stawów, łuszczyca plackowata, zesztywniające zapalenie stawów kręgosłupa, choroba Leśniowskiego-Crohna lub wrzodziejące zapalenie jelita grubego. Leki biologiczne, takie jak antagoniści receptora TNF-α, są stosowane, gdy żadne inne leki nie pomagają w wymienionych chorobach lub nie powodują zbyt wielu skutków ubocznych.
Preparaty biologiczne w zesztywniającym zapaleniu stawów kręgosłupa
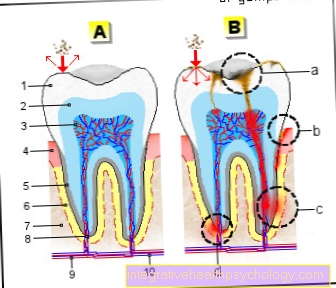
Choroba Bechterewa jest zapalną, przewlekłą chorobą autoimmunologiczną. Należy do reumatycznej grupy form. Jest to jeden z tak zwanych spondyloartropatii. W chorobie Bechterewa własny układ odpornościowy organizmu jest skierowany przeciwko komórkom kości i chrząstki w okolicy miednicy i pleców i niszczy je. Może to prowadzić do bólu stawów i deformacji odpowiednich obszarów ciała. W pewnych okolicznościach można również stosować antagonistów receptora TNF-α. Hamują substancję przekaźnikową TNF-α. Ponieważ ta substancja przekaźnikowa odgrywa główną rolę w procesie zapalnym, proces chorobowy jest blokowany przez hamowanie TNF-α. Może to złagodzić objawy i opóźnić postęp choroby.
Przeczytaj więcej na ten temat pod adresem: Terapia zesztywniającego zapalenia stawów kręgosłupa
Biologia na łuszczycę
Potoczna łuszczyca jest znana w żargonie technicznym jako łuszczyca plackowata. Objawia się silnym łuszczeniem się skóry ze swędzeniem i piekącym bólem. Może mieć różny stopień nasilenia. W przypadku nasilenia umiarkowanego do ciężkiego, czasami stosuje się antagonistów receptora TNF-α.
O tym nasileniu choroby mówi się, gdy dotyczy ponad 10% powierzchni skóry lub gdy zmiany skórne pojawiają się w szczególnie widocznych częściach ciała, takich jak dłonie lub twarz. Bardzo wysoki poziom cierpienia pacjenta jest również kryterium kwalifikacji do łuszczycy od umiarkowanej do ciężkiej. W niektórych przypadkach leki biologiczne mogą być już stosowane bez wszystkich innych składników aktywnych, które zawiodły lub nie trzeba było udowodnić obecności skutków ubocznych. Antagoniści receptora TNF-α mogą zahamować reakcje zapalne w momencie ich powstania, poprawiając w ten sposób jakość życia chorego pacjenta.
Ponadto w pewnym stopniu można zapobiegać chorobom wtórnym, które mogą wynikać z łuszczycy, takim jak depresja.
Przeczytaj więcej na ten temat pod adresem: Leczenie łuszczycy lub łuszczycy
Preparaty biologiczne na wrzodziejące zapalenie jelita grubego
Wrzodziejące zapalenie jelita grubego charakteryzuje się silnymi, przewlekłymi, przerywanymi procesami zapalnymi błony śluzowej jelita i leżącej poniżej warstwy tkanki łącznej. W ciężkich przypadkach tworzą się wrzody. W przeciwieństwie do choroby Leśniowskiego-Crohna, okrężnica jest dotknięta prawie wyłącznie. Również w tym typie choroby autoimmunologicznej antagoniści receptora TNF-α mogą pozytywnie wpływać na przebieg choroby. Obecnie zatwierdzono wiele różnych leków biologicznych do leczenia wrzodziejącego zapalenia jelita grubego.
Przeczytaj więcej na ten temat pod adresem: Terapia wrzodziejącego zapalenia jelita grubego
Biologia choroby Leśniowskiego-Crohna
Choroba Leśniowskiego-Crohna jest przewlekłą zapalną chorobą autoimmunologiczną. Własny system obronny organizmu skierowany jest przeciwko komórkom przewodu pokarmowego. Może to wpływać na cały układ pokarmowy, od jamy ustnej do odbytu. Tutaj TNF-α odgrywa rolę, ponieważ zapewnia wystąpienie procesów zapalnych i niszczenia komórek. Dlatego też inhibitory TNF-α mogą również hamować procesy chorobowe w kontekście choroby Crohna i częściowo zapobiegać następczym uszkodzeniom.
Przeczytaj więcej na ten temat pod adresem: Terapia choroby Leśniowskiego-Crohna
Biologia na reumatyzm
Wiele chorób ma charakter reumatyczny. Kiedy reumatyzm jest używany potocznie, jest to zwykle reumatoidalne zapalenie stawów. Jest to przewlekła zapalna choroba autoimmunologiczna, w której komórki odpornościowe niszczą komórki chrzęstne i kostne. Występuje ból i obrzęk stawów. Dzieje się tak często w okolicy stawów śródstopno-paliczkowych palców rąk i nóg. Często występuje sztywność poranna. Tutaj również modulator zapalenia TNF-α odgrywa główną rolę. Antagonistów receptora TNF-α można stosować w terapii reumatoidalnej, jeśli zawiodą inne środki.
Przeczytaj więcej na ten temat pod adresem: Terapia reumatoidalnego zapalenia stawów
Substancja czynna / działanie
Większość biologików to białka. Istnieją różne generacje leków biologicznych, a zatem także inhibitorów TNF-α. Pokolenia różnią się od producenta.
Końcówka nazwy pokazuje, ile białka mysiego jest nadal obecne w składnikach aktywnych. Z końcówką –omab jest to 100%, z końcówką –ximab nadal jest 25% mysiego białka, z końcówką - 5-10% jest nadal dostępne, a z końcówką –umab wcale. Odgrywa to rolę w tolerancji leków.
Ponadto inhibitory TNF-α mogą działać na różne sposoby. Mogą przechwytywać TNF-α, a tym samym zapobiegać wiązaniu się go z receptorem. W rezultacie w komórce nie zachodzą pewne procesy, które prowadziłyby do destrukcyjnej reakcji immunologicznej.Inną możliwością jest to, że inhibitor TNF-α blokuje miejsce wiązania TNF-α z receptorem. Lek działa wówczas jako tak zwany antagonista. Możliwe jest również, że inhibitory TNF-α działają jako tak zwane białka fuzyjne. Nazywa się je również receptorami wabików. Receptory wabików to receptory, które wiążą ligandy, ale nie przekazują sygnałów. Receptory wabika TNF-α są rozpuszczalnymi receptorami, które przechwytują TNF-α, zanim dotrze on do swojego pierwotnego miejsca przeznaczenia. W rezultacie nie ma już sygnału, a wzrost niszczących komórek odpornościowych jest spowolniony.
Enbrel®
Substancja czynna Etanercept jest obecna w handlowym preparacie Enbrel®. Jest to tak zwany receptor wabika lub białko fuzyjne. Enbrel® jest stosowany w szczególności przy reumatycznym zapaleniu stawów, młodzieńczym przewlekłym zapaleniu stawów, łuszczycowym zapaleniu stawów i tak zwanym zapaleniu stawów kręgosłupa. Łuszczycowe zapalenie stawów to szczególna postać łuszczycy, która wiąże się z bólem stawów. Enbrel® działa jako inhibitor TNF-α w tych chorobach, jak również w niektórych innych chorobach autoimmunologicznych. Jednak Enbrel® nie jest skuteczny w chorobie Leśniowskiego-Crohna. Z reguły podaje się go podskórnie raz w tygodniu po 50 mg lub dwa razy w tygodniu po 25 mg.
Przeczytaj więcej na ten temat pod adresem: Enbrel®
Remicade®
Substancję czynną infliksymab można znaleźć na przykład w handlowym preparacie Remicade®. Infliksymab jest chimerycznym przeciwciałem monoklonalnym, które blokuje aktywność TNF-α. Ponieważ jest to chimeryczne przeciwciało monoklonalne, główny szkielet jest ludzki, a miejsca wiązania antygenu (25%) to mysie białko. Oznacza to, że skuteczność jest wyższa niż w przypadku tak zwanych mysich przeciwciał monoklonalnych, które składają się w 100% z białka mysiego i niższa w porównaniu z przeciwciałami humanizowanymi (5-10% białka mysiego) lub ludzkimi przeciwciałami monoklonalnymi (0% białka mysiego). W związku z tym ryzyko alergii i nietolerancji jest niższe niż w przypadku mysich przeciwciał monoklonalnych i wyższe niż w przypadku przeciwciał humanizowanych lub ludzkich. Remicade® jest stosowany w reumatoidalnym zapaleniu stawów, łuszczycowym zapaleniu stawów, zesztywniającym zapaleniu stawów kręgosłupa i innych chorobach autoimmunologicznych. W przeciwieństwie do etanerceptu, aktywny składnik infliksymab jest również skuteczny w chorobie Leśniowskiego-Crohna. W zależności od choroby dawka wynosi 3-5 mg na kg masy ciała.
dawkowanie
Ponieważ bilogiki są zwykle białkami, należy je podawać pozajelitowo (we wlewie). Połknięcie doustne nie jest możliwe, ponieważ organizm by to strawił, a składniki aktywne nie mogły rozwinąć swojego działania. Dawkowanie zależy od substancji czynnej i występującej choroby. Dawka jest zwykle w zakresie od jednej do dwucyfrowych miligramów i jest podawana 1-2 razy w tygodniu.
Cena £
Koszt biologiki jest bardzo wysoki. Dlatego są one najczęściej używane tylko w ostateczności. To znaczy, jeśli wszystkie inne składniki aktywne, które są wskazane dla odpowiednich chorób, nie przyniosą rezultatu. Z reguły dwie strzykawki kosztują około 1600 euro miesięcznie.
Skutki uboczne
W ramach specjalistycznego leczenia i obserwacji blokery TNF-α są lekami stosunkowo dobrze tolerowanymi i bezpiecznymi. Jednak, podobnie jak w przypadku każdego leku, mogą wystąpić działania niepożądane. Skutki uboczne można podzielić na te związane ze stosowaniem leku i te związane z zaburzeniami układu odpornościowego. Ponieważ leki biologiczne muszą być podawane pozajelitowo (w postaci wlewu), teoretycznie mogą wystąpić reakcje związane z infuzją. W porównaniu z innymi lekami biologicznymi zdarza się to częściej w przypadku aktywnego składnika infliksymabu. Jednak przy leczeniu specjalistycznym tego typu działania niepożądane można zwykle dobrze kontrolować. Jeśli Biologikas zostanie podany podskórnie (pod skórę), mogą wystąpić miejscowe reakcje skórne. Jednak do tej pory przerwanie terapii było bardzo rzadko konieczne.
Efekty uboczne, które pojawiają się w wyniku ingerencji w układ odpornościowy, polegają na dodatkowym hamowaniu procesów fizjologicznych w naszym organizmie. Substancja przekaźnikowa TNF-α jest w rzeczywistości ważnym modulatorem zapalenia. Nawet jeśli jest częściowo skierowany przeciwko układowi odpornościowemu, ma ważne zadania związane z układem odpornościowym. Jeśli te ważne funkcje TNF-α są trwale blokowane przez leki, może to prowadzić do odpowiednich skutków ubocznych. Podatność na infekcje może wzrosnąć, a ryzyko raka może również wzrosnąć w przypadku długotrwałego stosowania. Może dojść do uszkodzenia wątroby, nerek i serca. Ponadto inhibitory TNF-α mogą reaktywować nieaktywną gruźlicę i półpasiec.
W zależności od generacji przeciwciał monoklonalnych ryzyko wystąpienia nietolerancji i alergii jest większe lub mniejsze. Oznacza to, że im więcej białka mysiego jest nadal obecne w substancji czynnej, tym większe jest ryzyko alergii i nietolerancji. Ponadto mogą wystąpić pewne autoprzeciwciała. Leczenie inhibitorem TNF-α rzadko prowadziło do tak zwanego tocznia rumieniowatego. To również zmniejszyło się ponownie, gdy zaprzestano podawania leku biologicznego. Ponadto opisano różne choroby i nawroty w kontekście stwardnienia rozsianego, a także pogorszenie w przypadku wyraźnej niewydolności serca.
interakcja
Jeśli podaje się szczepionki zawierające żywe szczepionki i jednocześnie z inhibitorami TNF-α, może to wywołać chorobę patogenem szczepionki zamiast efektu szczepienia. Ponadto można było zaobserwować interakcję podczas łączenia dwóch leków biologicznych. Na przykład zaobserwowano to przy jednoczesnym podawaniu etanerceptu i anakinry w trakcie leczenia reumatoidalnego zapalenia stawów. Efekt nie został poprawiony, ale skutki uboczne zostały wzmocnione. Rozwinęły się poważne infekcje i niedobór niektórych krwinek, tak więc rozwinęła się neutropenia.
Kiedy nie należy przyjmować leków biologicznych?
W przypadku wcześniejszej gruźlicy nie należy stosować inhibitorów TNF-α. Nie ma znaczenia, jak dawno temu chorowałeś na gruźlicę. Wynika to z faktu, że inaktywowane bakterie gruźlicy są nadal obecne w organizmie po tym, jak ktoś zachorował na gruźlicę. Te bakterie gruźlicy są nieaktywne, ponieważ czuwają nad nimi tzw. Makrofagi. Dbają, aby bakterie nie uaktywniły się ponownie. Aby makrofagi mogły wykonać to zadanie, potrzebują TNF-α. Jeśli makrofagi nie są już wystarczająco dostępne ze względu na działanie leku, nie mogą już wykonywać swojego zadania. W rezultacie bakterie gruźlicy mogą ponownie uaktywnić się i reaktywować gruźlicę.
Ponadto obecność wirusowego zapalenia wątroby typu B jest przeciwwskazaniem do leczenia czynnikiem biologicznym. Stwierdzono, że w tym przypadku leczenie inhibitorem TNF-α może reaktywować półpasiec. Przejawiało się to zwiększoną częstością występowania półpaśca i ospy wietrznej u dorosłych.
Jednak stwierdzono różnice w różnych składnikach czynnych inhibitorów TNF-α. Choroby te występowały częściej u pacjentów leczonych infliksymabem, podczas gdy te działania niepożądane były rzadko obserwowane podczas terapii etanerceptem. Poziom ryzyka reaktywacji korelował z wiekiem w obu chorobach, z tzw. Chorobami współistniejącymi (choroby dodatkowe) oraz z dodatkowym leczeniem glikokortykoidami, np. Kortyzonem.
Jednak w celu ochrony pacjenta obecnie jest tak, że leczenie inhibitorem TNF-α w przypadku przebytej gruźlicy lub wirusowego zapalenia wątroby typu B jest generalnie niedozwolone.
Biologie i alkohol - czy są kompatybilne?
Podczas leczenia środkami biologicznymi nie musisz całkowicie rezygnować z alkoholu. Istnieją jednak doniesienia z doświadczeń, w których opisano nietolerancje. Ponieważ leki biologiczne wpływają na funkcje nerek i wątroby, jest całkiem możliwe, że spożycie alkoholu może prowadzić do ostrej nietolerancji. Ponadto długotrwałe spożywanie alkoholu w połączeniu z lekami biologicznymi może zwiększać ryzyko chorób wątroby i nerek.
Koszt leczenia
Koszty są bardzo wysokie ze względu na proces wytwarzania i podawanie pozajelitowe. Koszt inhibitorów TNF-α wynosi około 40 000 do 50 000 euro rocznie. Pojedyncza aplikacja znajduje się co najmniej w górnym dwucyfrowym zakresie. Do tego dochodzą koszty personelu, koszty badań wstępnych itp. Jeżeli specjalista w przychodni lub klinice zdecyduje, że leczenie lekiem biologicznym jest najlepszą formą terapii, musi podać uzasadniony powód. Może złożyć wniosek do kasy chorych o pokrycie kosztów. Rozpatrzenie wniosku trwa zwykle kilka tygodni. Po sprawdzeniu, rozpatrzeniu i zatwierdzeniu wniosku ubezpieczyciel pokrywa koszty. Może jednak ograniczyć czas trwania przejęcia. Zobowiązanie finansowe jest często początkowo przyjmowane na 3 miesiące. Następnie należy złożyć nowy wniosek.
W 2016 roku oficjalnie zarejestrowano pierwsze tzw. Leki biopodobne do leczenia chorób reumatycznych. Jak sama nazwa wskazuje, są one podobne do Biologikas, ale nie takie same jak oryginał. Niektórzy autorzy sugerują, że są one tańszą alternatywą dla leków biologicznych. Jest kontrowersyjne, czy ich efekt faktycznie odpowiada efektowi oryginału. Ubezpieczenia zdrowotne mają nadzieję zaoszczędzić miliardy kosztów. Inni eksperci są sceptyczni wobec szacunków. Jak dotąd leki biopodobne były stosowane tylko u około 1-2% pacjentów z reumatyzmem. Leki biopodobne są zalecane przez Niemieckie Towarzystwo Reumatologiczne. Jednak odradza przejście z produktu oryginalnego na produkt zastępczy. Ponieważ nie ma jeszcze długoterminowych badań na ten temat, specjalistyczne społeczeństwo nie może jeszcze z zadowoleniem przyjąć takiej zmiany składników aktywnych. Odradza też podejmowanie takich decyzji wyłącznie ze względu na koszty. Ponadto jest zbyt optymistyczna, jeśli chodzi o ocenę oszczędności kosztów. Podsumowując, można powiedzieć, że mimo kosztów nie jest jeszcze możliwe oszacowanie, jak będzie wyglądać stosowanie leków biologicznych w przyszłości.